
Коллектив авторов
Миастения. Диагностика и лечение
УСЛОВНЫЕ СОКРАЩЕНИЯ
АлАТ – аланинаминотрансфераза
АМН – Академия медицинских наук
АсАТ – аспартатаминотрансфераза
АТ – антитело
АХ – ацетилхолин
АХР – ацетилхолиновые рецепторы
АХЭ – ацетилхолинэстераза
АХЭП – антихолинэстеразные препараты
БАС – боковой амиотрофический склероз
БД – безопасные дозы
ВЖ – вилочковая железа
ВОЗ – Всемирная организация здравоохранения
ГАК – газы артериальной крови
ГКС – глюкокортикостероиды
ГМ – генерализованная миастения
ГС – гемосорбция
ДЕ – двигательная единица
ДНК – дезоксирибонуклеиновая кислота
ЕД – единица действия
ЖЕЛ – жизненная емкость легких
ЖКТ – желудочно-кишечный тракт
ИВЛ – искусственная вентиляция легких
ИЛ – интерлейкин
ИФН – интерферон
КТ – компьютерная томография
КФК – креатинфосфокиназа
ЛДГ – лактатдегидрогеназа
ЛенГИДУВ – Ленинградский государственный институт усовершенствования врачей
МБк – мегабеккерель
МЕ – международная единица
МКБ-10 – международная классификация болезней, травм и причин смерти
10-го пересмотра
ММА – Московская медицинская академия
МР – магнитно-резонансный
МРТ – магнитно-резонансная томография
МСКТ – мультиспиральная компьютерная томография
НАД – никотинамиддинуклеотид
НМС – нервно-мышечный синапс
н-ХР – н-холинорецепторы
ОНМК – острое нарушение мозгового кровообращения
ОП – обменный плазмаферез
ПА – плазмаферез
ПД – потенциал действия
ПДДЕ – потенциал действия двигательной единицы
ПСМ – постсинаптическая мембрана
ПЭТ – позитронно-эмиссионная томография
РНК – рибонуклеиновая кислота
РФП – радиофармпрепарат
СЗГМУ – Северо-Западный государственный медицинский университет
СОЭ – скорость оседания эритроцитов
СПбМАПО – Санкт-Петербургская медицинская академия последипломного образования
ССЗ – сердечно-сосудистые заболевания
ТМ – тяжелая миастения
тРНК – транспортная рибонуклеиновая кислота
УЗИ – ультразвуковое исследование
УФ – ультрафиолетовый
УФО – ультрафиолетовое облучение
ФНО – фактор некроза опухоли
ЦВЗ – цереброваскулярные заболевания
ЦНС – центральная нервная система
ЧН – черепные нервы
ЭКГ – электрокардиограмма
ЭМГ – электромиография
ЭУФОЛК – экстракорпоральное ультрафиолетовое облучение лимфоцитов крови
ATA – anti-titin-antibody – антититиновые антитела
BiPAP – двухуровневая вентиляция с положительным давлением на вдохе
FDА – Food and Drug Administration – управление по санитарному надзору за качеством пищевых продуктов и медикаментов (США)
НLА – human leucocyte antigen – антиген лейкоцитов человека
НU – Haunsfield units – единицы шкалы Хаунсфилда
Ig – иммуноглобулины
IgG – иммуноглобулин G
MCD – mean of consecutive difference – среднее значение взаимосвязанных интервалов
МuSK – muscle specific receptor tyrosine kinase – мышечно-специфическая тирозинкиназа
SFЕМG – single-fibreelectromyography – электромиограмма одиночного мышечного волокна
ПРЕДИСЛОВИЕ
Бытует мнение, что миастения впервые была описана знаменитым английским анатомом Томасом Уиллисом (Thomas Willis) в 1672 г. В действительности же одной из первых публикаций стала работа сэра С. Уилкса (Sir Samuel Wilks), который в 1877 г. опубликовал заметку о больном с хроническим бульбарным параличом и летальным исходом болезни. При патологоанатомическом исследовании изменений в нервной системе выявлено не было. Позже вклад в изучение этого сложного заболевания внесли В. Эрб (1879), Г. Оппенгейм (1894), Уильям Говерс (1893). Однако кардинальный признак болезни – патологическая утомляемость мышц – был впервые изучен и описан в 1893 г. варшавским невропатологом С. Гольдфламом. В 1895 г. Ф. Жолли описал у больных миастенией тот же симптом патологической утомляемости мышц при раздражении их электрическим током, назвав это «миастенической реакцией электровозбудимости», и предложил название болезни «myasthenia gravis pseudoparalytica». К моменту появления в 1901 г. монографии Г. Оппенгейма «Миастенический паралич» в мировой литературе насчитывалось около 80 публикаций с описанием наблюдений этой болезни.
Отечественные ученые также внесли существенный вклад в изучение миастении, и среди первых были А. Я. Кожевников (1896), Г. И. Маркелов (1910) и многие другие. В 1960 г. впервые описана роль антител к ацетилхолиновым рецепторам постсинаптической мембраны нервно-мышечных синапсов в патогенезе миастении (J. Strauss). Миастения долго считалась тяжелым заболеванием с прогрессирующим течением и неблагоприятным прогнозом, летальность при ней достигала 40 %. С середины ХХ в. ситуация стала изменяться в лучшую сторону благодаря разработке новых способов патогенетического лечения.
Миастения относится к числу заболеваний, способных поражать людей всех возрастов – детей, взрослых и стариков, однако чаще заболевают женщины в возрасте 20 – 40 лет. В наш век глобализации, урбанизации и интенсификации всех сторон жизни наблюдается повсеместный рост заболеваемости аутоиммунными болезнями, к которым относится и миастения. В настоящее время популяционная частота миастении составляет около 5 – 10 человек на 100 000 жителей. Несмотря на достаточно полное описание клинических форм и наличие современных методов исследования, практические врачи продолжают испытывать сложности при диагностике миастении. Ее путают с острыми нарушениями мозгового кровообращения, преимущественно в вертебрально-базилярном бассейне, менингитами, поражениями глазодвигательных нервов и многими другими недугами.
С момента опубликования первой в нашей стране монографии на русском языке, посвященной миастении (Лобзин В. С., 1960), минуло 54 года. Представления об этиологии, патогенезе и подходах к лечению этого заболевания дополнились современными многочисленными исследованиями, накоплен существенный опыт в его диагностике и патогенетическом лечении.
Выпуск данной монографии авторы считают необходимым по двум основным причинам. Первая – почтить память заслуженного деятеля науки Российской Федерации профессора Владимира Семеновича Лобзина в связи с его заслугами в области изучения миастении в нашей стране и в связи с 90-летием со дня его рождения (28.09.2014 г.).
В. С. Лобзин – воспитанник Военно-морской медицинской академии, ученик знаменитых профессоров – Александра Викторовича Триумфова, автора настольной книги каждого невролога «Топическая диагностика заболеваний нервной системы», и Александра Гавриловича Панова – блестящего клинициста и ученого, открывшего миру клещевой энцефалит.
Владимир Семенович после окончания факультета руководящего состава ВММА был вначале направлен для практической службы-работы в Кронштадтский военно-морской госпиталь, а позже переведен в 1-й Военно-морской ордена Ленина госпиталь в Ленинграде. Еще в период обучения в ВММА, а затем службы в военно-морских госпиталях Владимир Семенович по совету профессора А. Г. Панова увлекся проблемой миастении, начал собирать материал для диссертации (защищена в 1957 г.) и готовить монографию «Миастения». Приглашение на кафедру нервных болезней Военно-медицинской академии (1964 г.) не было случайным: Владимир Семенович обладал уже серьезным практическим опытом, был кандидатом медицинских наук, крупным специалистом в изучении миастении. Большой интерес к этой проблеме Владимир Семенович сохранил на протяжении всей своей жизни. Кафедра и клиника нервных болезней им. М. И. Аствацатурова Военно-медицинской академии именно благодаря В. С. Лобзину стала «нервно-мышечной Меккой» и первым, правда неофициальным, Всесоюзным центром изучения миастении (1971 г.). Со всех концов необъятной Советской страны в Академию к В. С. Лобзину стали стекаться сотни больных миастенией в надежде найти помощь и облегчение своим страданиям. Именно там, в Академии, под руководством А. Г. Панова разрабатывались новые эффективные способы диагностики и лечения этой тяжелейшей болезни. Исследования В. С. Лобзина по этой проблеме были продолжены на кафедре нервных болезней ЛенГИДУВа – СПбМАПО. После избрания на должность заведующего кафедрой невропатологии ЛенГИДУВа Владимир Семенович на протяжении 10 лет являлся заместителем председателя Всесоюзного центра по нервно-мышечной патологии. Председателем его в те годы был академик АМН СССР Л. О. Бадалян. Владимир Семенович плодотворно сотрудничал и был в дружеских отношениях с создателем Всесоюзного миастенического центра в Москве (1983) профессором Б. М. Гехтом.
В. С. Лобзин, прославившийся очень глубокими исследованиями в самых различных областях клинической неврологии (нейроинфекции, неврозы и астенические состояния, аутогенная тренировка, болезни периферической нервной системы, эпилепсия, экстремальная и военная неврология и др.), внес наиболее существенный вклад в разработку проблемы миастении. Им разработаны клинические тесты диагностики этого заболевания, впервые предложено описание симптома «генерализации мышечного утомления при миастении» (1960), ныне известного как симптом В. С. Лобзина, изучены новые аспекты патогенеза, впервые в стране применен для диагностики поражений вилочковой железы радионуклидный метод исследования, определение антител к холинорецепторам (совместно с В. А. Смирновым и Л. А. Сайковой), предложены и испытаны различные методы дифференцированной терапии, в том числе при миастении у детей. Комплексный подход к разработке этой проблемы, осуществленный совместно с хирургами (В. Н. Васильевым, М. А. Лущицким, Г. А. Макиенко), анестезиологами (В. Л. Ваневским), иммунологами, позволил в значительной степени повысить эффективность лечения этого тяжелого заболевания. Под руководством В. С. Лобзина проводилась большая работа по внедрению эфферентной терапии при лечении больных миастенией. Профессор В. С. Лобзин являлся ведущим специалистом по миастении не только в нашей стране, его многочисленные труды известны и за рубежом. Знаменитый нейромиолог Ирена Гаусманова-Петрусевич прислала В. С. Лобзину на редактирование первый номер международного журнала «Нервно-мышечные болезни» и просила его войти в состав редакционной коллегии. Вопросы изучения миастении изложены В. С. Лобзиным в монографии «Миастения» (1960), в 41 статье, а также в вышедшей уже после его смерти монографии «Миастения у детей» (совместно с Н. М. Жулевым и Л. Н. Дементьевой, 2001). По этой проблеме под руководством В. С. Лобзина выполнены 4 кандидатских и 1 докторская диссертации. В. С. Лобзин неоднократно участвовал во всесоюзных конференциях и съездах, международных симпозиумах, выступая с докладами, посвященными различным аспектам диагностики и лечения миастении.
Второй причиной, побудившей авторов взяться за подготовку данной монографии, явилась необходимость ознакомления широкого круга практических врачей с современными подходами к диагностике и патогенетическому лечению миастении на основании собственного значительного клинического опыта (кафедры неврологии им. акад. С. Н. Давиденкова) и самых современных опубликованных сведений.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ МИАСТЕНИИ
На основании большого личного опыта и данных современных публикаций, авторы дают характеристику клинической картины, диагностики и системы комплексного лечения миастении.
Клиника нервных болезней Ленинградского государственного института усовершенствования врачей им. С. М. Кирова, преобразованного затем в Санкт-Петербургскую медицинскую академию последипломного образования и впоследствии – в Северо-Западный медицинский университет, занимается изучением миастении с 1945 г. С. Н. Давиденков настойчиво изыскивал новые методы лечения этого заболевания. Так, впервые в Советском Союзе по его предложению в 1958 г. А. С. Чечулиным в 1-й хирургической клинике ЛенГИДУВа была успешно произведена тимэктомия у больного миастенией.
Систематическое изучение миастении, проводившееся на протяжении более 40 лет, позволило сотрудникам кафедры неврологии им. акад. С. Н. Давиденкова Северо-Западного государственного медицинского университета им. И. И. Мечникова, авторам этой монографии, к настоящему времени накопить опыт, во многом приоритетный (С. Н. Давиденков, Л. В. Догель, В. С. Лобзин и др.). Для распознавания миастении у взрослых и детей выявлен ряд патогномоничных феноменов, предложены оригинальные клинические и диагностические тесты и приемы. Разработаны и внедрены новые способы диагностики и дифференциации миастении от офтальмоплегии иной этиологии путем использования импедансометрии акустического стапедиального рефлекса в сочетании с фармакологическими пробами (Лобзин В. С., Жулев Н. М. [и др.], 1989).
Произведена сравнительная оценка активности антихолинэстеразных препаратов (АХЭП) у взрослых и детей (Догель Л. В., 1947–1990; Лобзин В. С., 1957–1990; Дементьева Л. Н., 1968–1986); изучены иммунологические аспекты патогенеза и лечения миастении у взрослых и детей; испытаны иммунодепрессанты и иммуномодуляторы (Лобзин B. C. [и др.], 1986). Доказан положительный эффект гемосорбции (ГС) у больных в предкризовых и кризовых состояниях (Лобзин B. C., Жулев Н. М. [и др.], 1986).
Впервые в нашей стране в 1981 г. предложен метод радионуклидной диагностики активности вилочковой железы (ВЖ) (Лобзин В. С. [и др.], 1981, 1983, 1989).
В настоящее время сотрудники кафедры нервных болезней продолжают интенсивно изучать миастению, разрабатывают новые методы диагностики и лечения в различных возрастных группах. Это необходимо и актуально, так как до настоящего времени у нас в стране и за рубежом остается много нерешенных вопросов, относящихся к проблеме данного заболевания.
Разнообразие начальных симптомов приводит к тому, что больные миастенией на первых этапах болезни нередко обращаются за помощью к врачам различных специальностей, недостаточная осведомленность которых относительно особенностей этого патологического состояния может привести к трагическим ошибкам.
Миастения (myasthenia gravis pseudoparalytica) – тяжелое нервно-мышечное заболевание с прогрессирующим течением, главным клиническим проявлением которого является патологическая утомляемость мышц, приводящая к парезам и параличам.
Заболевание может возникнуть в любом возрасте: с первого года жизни до глубокой старости. Чаще всего (75 % больных) миастения наблюдается в молодом возрасте – от 15 до 30 лет. По данным отечественных и зарубежных авторов, женщины болеют в 2–3 раза чаще мужчин. Это согласуется с результатами, полученными на кафедре неврологии им. акад. С. Н. Давиденкова.
Впервые эта своеобразная клиническая форма была описана более ста лет назад – в 1877 г. – и долго считалась очень редким заболеванием. В настоящее время отмечается четкая тенденция к увеличению заболеваемости миастенией. Частота заболевания варьирует, по данным разных авторов и в разных странах, от 0,5 до 5 случаев на 100 000 жителей.
Заболевание не имеет специфического географического распределения и встречается в разных частях света независимо от клинических условий и этнографического фактора.
В 1901 г. K. Weigert и L. Laquer обнаружили при аутопсии злокачественную опухоль (типа саркомы) ВЖ у больного, погибшего от миастении. Описание этого наблюдения ознаменовало начало представлений о связи миастении с поражением ВЖ.
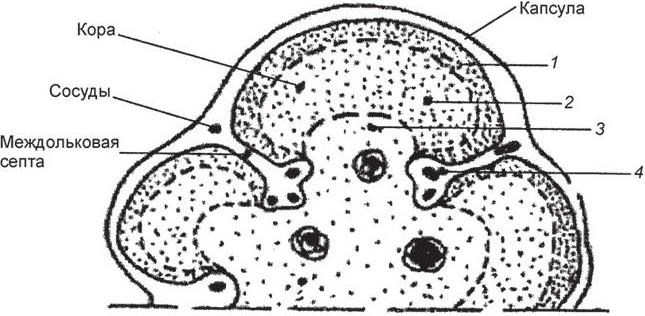
Рис. 1. Структурно-функциональные зоны вилочковой железы (по: Харченко В. П. [и др.], 1998):
1 – субкапсулярная; 2 – внутренняя кортикальная; 3 – медуллярная; 4 – внутридольковые периваскулярные пространства
С тех пор многие ученые, признавая роль ВЖ в патогенезе миастении, до сих пор ссылаются на работу K. Weigert и L. Laquer как на приоритетную.
Вилочковая железа (thymus) состоит из лимфоидной и эпителиальной ткани. В ней выделяют 4 структурно-функциональные зоны (Ивановская Т. Е. [и др.], 1996):
1) субкапсулярная зона, где происходит «встреча» пре-Т-лимфоцитов с нелимфоидным компонентом ВЖ, пролиферация и ранние этапы созревания Т-лимфоцитов;
2) внутренняя кортикальная зона, где под влиянием прямого контакта с эпителием и макрофагами, несущими антигены I и II классов сиcтемы HLA, под влиянием гуморальных факторов, в том числе гормонов ВЖ, интерлейкинов (ИЛ), происходит дальнейшее созревание Т-лимфоцитов и становление аутотолерантности; при этом апоптозу подвергаются 95 % и более Т-лимфоцитов; микроокружение представлено эпителиальными клетками и макрофагами;
3) медуллярная зона, где расположены зрелые Т-лимфоциты и, вероятно, происходит их антигензависимое созревание в контакте с эпителиальными и интердигитирующими клетками под влияниями гормонов ВЖ, ИЛ; микроокружение представлено медуллярным эпителием, интердигитирующими клетками и макрофагами; а также миоидными клетками – единственными клетками ВЖ, несущими ацетилхолиновые рецепторы (АХР) на своей мембране (Kirchner T. [et al.], 1988; Kaminski H. J. [et al.], 1993, цит. по: Кузин М. И., Гехт Б. М., 1996);
4) внутридольковые периваскулярные пространства, соответствуют по своей структуре и функции периферической лимфоидной ткани; в области кортико-медуллярной границы они обеспечивают транспорт лимфоцитов, в корковом веществе – являются компонентом гемато-тимического барьера (рис. 1).
Изменениям ВЖ при миастении у взрослых посвящено много работ, но описания изменений ее у детей, больных миастенией, крайне редки. Общепризнанно, что при миастении у детей обнаруживается гиперплазия ВЖ (Гаджиев С. А. [и др.], 1971; Коган О. Г. [и др.], 1980; Копьева Т. Н. [и др.], 1986; Bundey S., 1972; Nissipeanu P. 1973).
При оценке структурных изменений в ВЖ детей, страдающих миастенией, необходимо учитывать ее морфологические изменения при так называемой акцидентальной инволюции и возрастной перестройке ткани железы (Кемилева З., 1983; Попов М. С. [и др.], 1983; Ивановская Т. Е. [и др.], 1996).
Уже в 10-летнем возрасте в ВЖ находят признаки возрастной инволюции в виде постепенного уменьшения объема коркового вещества при относительном увеличении мозгового вещества. В последнем увеличивается количество тимических телец, они начинают подвергаться гиалинозу и кальцинозу с явлением укрупнения. Количество тимоцитов уменьшается, разрастается соединительная и жировая ткань, и к 50–60 годам ВЖ представляет собой остаточное жировое образование с островками паренхимы и кальцинированными тимическими тельцами (Ивановская Т. Е. [и др.], 1978).
Т. Н. Копьева и С. М. Секамова (1990), на основании гистологических, гистохимических и электронно-микроскопических исследований ВЖ при миастении у детей, делают вывод о значительной активности эпителиальных клеток железы при ювенильной миастении. Высказывается предположение о том, что положительный эффект тимэктомии при миастении в определенной степени связан с повышенной функциональной активностью железы.
Мы провели сравнительное изучение морфологического строения ВЖ у взрослых больных и больных миастенией детей. При этом выявлено следующее:
– несмотря на возраст, у 11,7 % детей обнаружены атрофические изменения ВЖ;
– в ВЖ чаще встречаются зародышевые центры;
– чаще отмечались гиперплазия мозгового слоя и нарушение взаимоотношения слоев в дольке;
– участки свежих кровоизлияний наблюдались с одинаковой частотой, но у детей превосходили по площади;
– в большем количестве обнаруживались плазматические и тучные клетки;
– размеры, форма и функциональное состояние телец вилочковой железы отличались у детей большой вариабельностью; такие явления, как распад, кистозное перерождение, у детей встречались чаще, реже наблюдался кальциноз телец вилочковой железы.
В настоящее время доказано, что миастения – аутоиммунное заболевание, развитие которого обусловлено АТ-опосредованной дисфункцией н-холинорецепторов (н-ХР) постсинаптической мембраны (ПСМ) нервно-мышечного синапса (НМС). Нарушение синаптической передачи связано с патологическими изменениями ВЖ, которая ответственна за иммунные реакции организма. Несмотря на то что изучением миастении занимаются в последние годы не только клиницисты, но и иммунологии, патофизиологи, специалисты по функциональной диагностике, биохимики, фармакологи, этиологические факторы миастенических реакций не уточнены. Не изучена последовательная цепь событий от внедрения первичного этиологического агента до формирования механизма патологических иммунных реакций. Существуют предположения, что миастения – это индуцированное вирусом иммунодефицитное состояние, и тогда могут быть оправданы попытки применения не мммунодепрессантов, а иммуномодуляторов. Речь идет о повреждающем действии аутоАТ на клеточные структуры ВЖ и на н-ХР, т. е. агрессивных аутоАТ, первично направленных на комплексы «вирус – клетка» («новый антиген», «псевдовирус») локализующихся в ВЖ. В этом случае показана иммунодепрессивная терапия.
Согласно гипотезе Н. Wekerle и H. Retelsen (1977), H. Wekerle и соавт. (1981), этиология и патогенез миастении рассматриваются следующим образом: имеющиеся в ВЖ стволовые клетки в результате воздействия неизвестного фактора (возможно, вируса) превращаются в миойдные клетки, Т-лимфоциты ВЖ сенсибилизируются к вновь дифференцированным миойдным клеткам, АХР. Эти антитела (АТ) перекрестно взаимодействуют с АХР скелетной мускулатуры и блокируют их. В результате возникают нарушения нервно-мышечной передачи. Т-лимфоциты превращаются либо в клетки-киллеры, разрушающие нервно-мышечную передачу, либо в клетки-хелперы, участвующие в образовании АТ к АХР.
Американский невропатолог М. Уокер (1934) выявила сходство клинической картины миастении с симптомами частичного отравления ядом кураре. Кураре вызывал быстрый паралич поперечно-полосатых мышц и диафрагмы, что приводило к остановке дыхания и смерти животных, за которыми охотились индейцы, применявшие отравленные стрелы. Частичная блокада нервно-мышечной передачи наступала и у людей, случайно или преднамеренно раненных стрелами, покрытыми этим ядом.
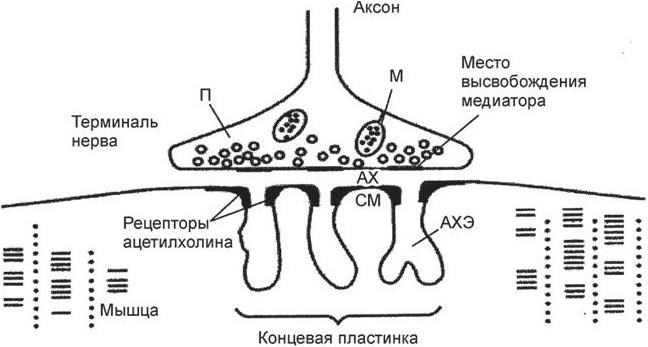
Рис. 2. Схематическое изображение нервно-мышечного соединения (по: Drachman D. B., 1998):
П – пузырьки с медиатором; М – митохондрии; СМ – складки ПСМ
М. Уокер наблюдала улучшение состояния таких пострадавших после введения им АХЭП физостигмина (эзерина). Предположив сходство клинической картины, этиологии и патогенеза параличей у отравленных кураре и у больных миастенией, М. Уокер получила «драматический эффект» в виде значительного улучшения состояния больных миастенией после введения физостигмина. Убедившись в отчетливом терапевтическом эффекте, М. Уокер пришла к выводу о гуморальном происхождении миастенического симптомокомплекса. Она считала, что мышцы больных миастенией при сокращении выделяют в кровь патологический продукт обмена, действующий аналогично яду кураре и блокирующий нервно-мышечную передачу.
Некоторые авторы предполагали, что это патологическое вещество продуцируется ВЖ. Очевидно, что в этом случае миастенические расстройства обусловлены конкурентной постсинаптической блокадой. С этого момента резко улучшились состояние и перспективы изучения больных миастенией.
В настоящее время установлено, что нарушение нервно-мышечной передачи при миастении выражается в конкурентной курареподобной блокаде в результате недостатка деполяризации ПСМ. При этом типе блокады рецептивная субстанция синапса становится невосприимчивой или заблокированной в отношении действия (контакта) ацетилхолина (АХ). Эта субстанция конкурентно связана с аутоагрессивными АТ к АХР. АХ оказывается недоступным для преодоления этой блокады. АХЭП связывают фермент ацетилхолинэстеразу (АХЭ), разрушающую избыток АХ. В результате АХ накапливается в области синапса в количестве, достаточном для преодоления блокады. Схематическое изображение нервно-мышечного соединения представлено на рис. 2.
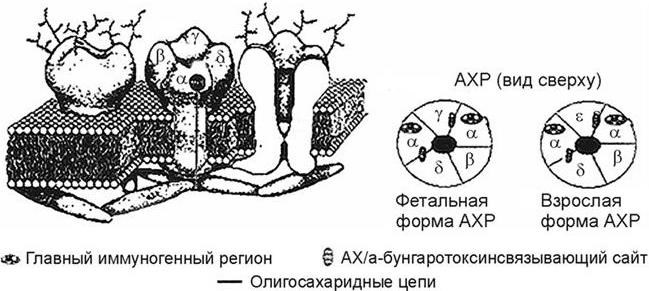
Рис. 3. Строение ацетилхолинового рецептора
АХР – основные поражаемые мишени при миастении, могут рассматриваться как преобразователи сигнала (Hucho F., 1992), функцией которых является передача внеклеточных сигналов внутрь клетки. Для АХР лигандом является нейромедиатор АХ, под действием которого происходит деполяризация плазматической мембраны. АХР принадлежит к суперсемейству лигандуправляемых ионных каналов (рис. 3). Этот рецептор состоит из пяти субъединиц, аминокислотная последовательность которых установлена на основании клонирования и секвенирования к дезоксирибонуклеиновой кислоте (ДНК) в 80-х годах прошлого века в лабораториях M. Noda и соавт. (1982, 1983), T. Claudio и соавт. (1983).


