Марина Команденко
Вирусные гепатиты у больных, подвергающихся диализу
УСЛОВНЫЕ СОКРАЩЕНИЯ
АГ – артериальная гипертензия
АлАТ – аланинаминотрансфераза
анти-НВс – антитела к НВс-антигену вируса гепатита В
анти-НВс IgM – антитела к НВс-антигену вируса гепатита В класса IgM
анти-НВе – антитела к НВе-антигену вируса гепатита В
анти-НВs – антитела к поверхностному антигену
анти-ВГС – антитела к вирусу гепатита С
анти-ВГЕ – антитела к вирусу гепатита Е
АсАТ – аспартатаминотрансфераза
ВГВ – вирусный гепатит В
ВГС – вирусный гепатит С
ВИЧ – вирус иммунодефицита человека
ГГТП – гамма-глютамилтранспептидаза
ДНК – дезоксирибонуклеиновая кислота
ЗПТ – заместительная почечная терапия
ИБС – ишемическая болезнь сердца
ИФА – иммуноферментный анализ
МАУ – микроальбуминурия
МЕ – международные единицы
МКБ-10 – Международная классификация болезней, 10-й пересмотр
ОВГ – острый вирусный гепатит
ОГВ – острый гепатит В
ОГС – острый гепатит С
ПТГ – посттрансфузионный гепатит
ПЦР – полимеразная цепная реакция
РНК – рибонуклеиновая кислота
СД – сахарный диабет
СКФ – скорость клубочковой фильтрации
тХПН – терминальная хроническая почечная недостаточность
УЗИ – ультразвуковое исследование
ХБП – хроническая болезнь почек
ХВГВ – хронический вирусный гепатит В
ХВГС – хронический вирусный гепатит С
ХГВ – хронический гепатит В
ХГС – хронический гепатит С
ХПН – хроническая почечная недостаточность
ХОБЛ – хроническая обструктивная болезнь легких
ХСБ – хронические сосудистые болезни
ЩФ – щелочная фосфатаза
СDC – центр по контролю за инфекционными заболеваниями, США
СМV – цитомегаловирус
EASL – Европейская ассоциация по изучению печени
GBV – вирус гепатита G
НbA1c – гликозилированный гемоглобин
HBcAg — сore-антиген вируса гепатита В
НВеАg – е-антиген вируса гепатита В
НВsAg – «s» – поверхностный антиген вируса гепатита В
HDAg – дельта-антиген
HDV – вирус гепатита D
HLA – человеческий лейкоцитарный антиген
IgM – иммуноглобулин М
IL-2 – интерлейкин 2
KT/V – индекс дозы диализа
L180M – мутация – замена лейцина на метионин
М204V и М204I – мутации валина и изолейцина в локусе гена
MDRD – модификация диеты при почечной болезни
RIBA – рекомбинантное исследование в иммуноблотинге
SENV – вирус гепатита SEN
TTV – вирус, передающийся при трансфузиях крови
UMDD – мутация вируса на фоне лечения ламивудином
ВВЕДЕНИЕ
Технический прогресс обусловил внедрение новых технологий в медицинскую практику. В последние годы широкое применение методов эфферентной терапии в лечебной практике в целях коррекции острых и хронических патологических состояний привело к возникновению различных осложнений этой терапии. Прежде всего, к ним относятся инфекционные заболевания, в том числе вирусные гепатиты, ВИЧ-инфекция (вирус иммунодефицита человека), гнойно-септические состояния. По мнению некоторых ученых, пациенты гемодиализа относятся к группе высокого риска заражения различными, особенно иммунокомпромиссными, заболеваниями. В связи с этим первостепенное значение приобретают вопросы обеспечения эпидемической безопасности пациентов и персонала при использовании методов эфферентной терапии и гемокоррекции (Шведов А. К. [и др.], 2001).
К методам эфферентной терапии относятся гемодиализ, плазмаферез, плазмосорбция, цитоферез, криоферез, криоплазмосорбция, гемосорбция и др. Из-за высокой степени инвазивности они могут играть важную эпидемиологическую роль в распространении инфекций в стационарах и учреждениях амбулаторного профиля (Нечаев В. В. [и др.], 1993).
Особенно часто заражение инфекциями происходит в отделениях диализа, плазмафереза стационаров, учреждений переливания крови. В литературе описаны и многочисленные вспышки, и единичные, спорадические заболевания, обусловленные вирусами гепатитов В, С, G, вирусом, передающимся при трансфузиях крови (TTV), ВИЧ-инфекцией и другими патогенными и условно-патогенными микроорганизмами.
Высокие уровни инфицированности вирусами гепатита В, С и другими патогенами выявляются у пациентов отделений диализа и трансплантации, гематологии, эндокринологии, туберкулеза, в хирургических, гастроэнтерологических, нефрологических, психиатрических, ортопедических, инфекционных и других отделениях, где проводится лечение методами эфферентной терапии.
Противоэпидемическое обеспечение эфферентной терапии недостаточно разработано. Практическая служба не располагает научно обоснованной системой профилактики заражений в центрах диализа, трансплантации, гемокорригирующей терапии, а в отделениях, где введены в практику методы эфферентной терапии, профилактика инфицирования проводится недостаточно эффективно (Нечаев В. В. [и др.], 2002).
Общие представления о хронических заболеваниях почек
В последнее десятилетие подходы к проблеме хронических заболеваний почек, ведущих к почечной недостаточности, претерпели ряд кардинальных изменений. Предпосылками послужили серьезные медико-социальные проблемы: увеличение общего числа больных, получающих заместительную почечную терапию (ЗПТ), дефицит информации о распространенности болезней почек, несвоевременная диагностика и запоздалая профилактика поражения почек, низкий уровень информированности населения о роли почечных функций в поддержании общего здоровья.
При проведении эпидемиологических обследований (Национальное исследование здоровья и питания 1999 – 2000 гг., США; NHANES – The National Health and Nutrition Examination Survey, USA) было отмечено, что информированность пациентов о наличии у них болезни почек довольно низкая. Даже если скорость клубочковой фильтрации (СКФ) оценивалась ниже 60 мл/мин, об имеющемся заболевании почек знали не более 10 % больных. Особенно актуально это оказалось для женщин, у которых низкий уровень креатинина сыворотки чаще всего маскирует истинные величины СКФ (Coresh J. [et al.], 2005).
О неудовлетворительной диагностике степени снижения почечных функций на начальных стадиях поражения паренхимы почек свидетельствует и факт непропорционального увеличения во всем мире числа больных с терминальной стадией хронической почечной недостаточности (тХПН), нуждающихся в ЗПТ, в сравнении с практическим неизменным общим количеством нефрологических больных. Об этом же свидетельствует и практика работы Санкт-Петербургского городского нефрологического центра, где в течение последних 30 лет регистрируется вся информация о нефрологических больных. До 50 % пациентов, получающих ЗПТ, наблюдаются у нефролога меньше одного года (Команденко М. С. [и др.], 2009).
Таким образом, значительная часть нефрологических больных теряют возможность получить своевременное лечение, хотя, по данным солидных многоцентровых исследований, именно оно позволяет значительно замедлить снижение СКФ и на несколько лет отодвинуть начало дорогостоящей ЗПТ (Jones C. [et al.], 2006).
Не менее важную роль в изменении подхода к проблеме хронической почечной патологии сыграло накопление доказательной базы данных, которая свидетельствует о роли поражения почек в прогрессировании сердечно-сосудистых болезней. Было показано, что поражение почек гораздо чаще регистрируется у лиц, страдающих сахарным диабетом (СД) и артериальной гипертензией (АГ). Исследования этих больных выявили связь между развитием признаков поражения почек и возрастанием частоты тяжелых сердечно-сосудистых осложнений. Исследования показали, что повышение риска смерти от сердечно-сосудистой патологии у пациентов с хронической болезнью почек (ХБП) возрастает в 10 – 20 раз по сравнению с контрольной группой, стратифицированной по полу и возрасту, а у молодых людей этот показатель увеличивается в 70 раз (Weiner D. E. [et al.], 2004).
Таким образом, вероятность получения заместительной почечной терапии у лиц с ХБП оказалась в 20 – 70 раз ниже, чем вероятность летального исхода из-за сердечно-сосудистой патологии (Foley R. N. [et al.], 2005) и подавляющее большинство больных, страдающих сердечно-сосудистыми заболеваниями, сопровождающимися поражением почек, погибает раньше, чем начинается ЗПТ. Доказательство единых механизмов развития, высокая социально-экономическая значимость АГ, ишемической болезни сердца (ИБС), СД и болезней почек позволили объединить их под общим названием «хронические сосудистые болезни» (ХСБ).
Однако в 2002 г., еще до появления понятия ХСБ, в целях достижения преемственности ведения больных с признаками поражения почек и оптимального взаимодействия между врачами различных специальностей рабочая группа Национального почечного фонда США опубликовала руководство, в котором были предложены новые концепции диагностики, классификации и сам термин «хроническая болезнь почек» (ХБП). Данный термин подразумевает наличие структурных или функциональных признаков повреждения почек, сопровождающихся или не сопровождающихся снижением СКФ, существующих в течение 3 мес. и более вне зависимости от нозологического диагноза. Это понятие не противоречит кодированию болезней, предложенному в Международной классификации болезней после 10-го пересмотра (МКБ-10). Основные положения предложенного руководства по ХБП включали в себя валидную диагностику, которую можно проводить независимо от этиологии, и классификацию тяжести ХБП, основанную на динамическом исследовании величин СКФ.
После внедрения новой классификации ХБП предполагалось унифицировать терминологию болезней почек и реже использовать понятие «хроническая почечная недостаточность», для обозначения которого в мировой литературе не было единого, общепринятого термина. Основные предложения о введении в нефрологию и практическую медицину понятия ХБП, по аналогии с понятиями «ишемическая болезнь сердца» (ИБС) или «хроническая обструктивная болезнь легких» (ХОБЛ), были поддержаны широким мировым нефрологическим сообществом и рекомендованы для внедрения в медицинскую практику в 2005 г. на VI съезде Научного общества нефрологов РФ. Необходимо отметить, что сегодня проводятся исследования в целях дальнейшей адаптации классификации ХБП к нуждам практического здравоохранения: разделение на подстадии, дополнение ее буквенными индексами, детализирующими клинические, лабораторные проявления болезни и методы ЗПТ (Levey A. S. [et al.], 2005; Смирнов А. В. [и др.], 2008). Но, несмотря на продолжающуюся работу в этом направлении, базисная, социальная сущность рассматриваемой проблемы остается неизменной.
Вирусные гепатиты в отделениях гемодиализа
Гемоконтактные вирусные гепатиты – одна из наиболее масштабных проблем здравоохранения во всех странах мира. Глобальность проблемы определяется не только широкой распространенностью заболеваний во всех формах их проявления в общей популяции населения (вирусным гепатитом В (ВГВ) инфицировано от 350 до 400 млн чел., а вирусным гепатитом С (ВГС) – 170 млн чел.), но и среди пациентов различных стационаров, в том числе отделений и центров диализа. Определено, что от 8 до 10 % больных, подвергавшихся диализу, инфицированы вирусом гепатита С (Tokars J. J. [et al.], 2000; Saab S. [et al.], 2001).
Известны, по крайней мере, шесть нозологических форм вирусных гепатитов, которые могут поражать пацентов и медицинский персонал отделений и цетров гемодиализа. К ним относятся вирусные гепатиты, передающиеся через кровь и другие секреты организма: В, С, D, G, TTV и вирус гепатита SEN (SENV).
Глава 1
ВИРУСНЫЙ ГЕПАТИТ В
1.1. Распространенность вирусного гепатита В в отделениях диализа
С момента выявления австралийского «s» – поверхностного антигена вируса гепатита В (HВsAg) – маркера вируса гепатита В прошло более 40 лет. Уже с конца 1960-х гг. стало известно, что в отделениях хронического диализа существует повышенный риск заражения пациентов гепатитом В. Пациенты и персонал отделений хронического диализа относятся к группам с высоким риском заражения вирусом гепатита В (Васильева В. И. [и др.], 1986; Нечаев В. В. [и др.], 1989; 1990; 2003а; Ивашкин И. Т. [и др.], 1993; Зубкин М. Л. [и др.], 2000; London W. T. [et al.], 1977; Alter M. J., 1986).
По мнению ряда отечественных и зарубежных исследователей, эпидемический процесс ВГВ в центрах хронического гемодиализа развивается интенсивно, проявляется преимущественно в виде безжелтушных форм, носительства вируса, реже – с клиническими симптомами заболевания, сопровождающегося желтухой.
По результатам скрининга отсутствие маркеров ВГВ и ВГС отмечается у 90 – 95 % больных, поступающих на программный гемодиализ. В процессе лечения и обследования 125 пациентов НВsAg обнаружен у 29 чел. (23,2 %), в том числе у 19,2 % – е-антиген вируса гепатита В (НВеАg) и у 40,8 % – антитела к поверхностному антигену (анти-НВs) (Акимкин В. Г. [и др.], 2000).
Серологический контроль за пациентами отделений гемодиализа показывает, что в среднем ежегодно в центрах хронического гемодиализа США инфицируется 1,0 % больных и 2,0 % персонала (Alter M. J. [et al.], 1983). Описаны многочисленные вспышки ВГВ с вовлечением в эпидемический процесс от 18,0 до 41,0 % больных и от 2,0 до 11,0 % персонала центра (Collste L. G., 1971; [et al.]). Однако весьма редко встречаются описание и анализ вспышек в условиях внедрения правил противоэпидемического режима и проведения профилактических прививок пациентам. Чаще всего речь идет о спорадической заболеваемости, развивающейся на фоне скрыто протекающего эпидемического процесса гепатита В, выявляемого обнаружением у пациентов основного маркера вируса – НВsAg или антител к различным антигенам вируса.
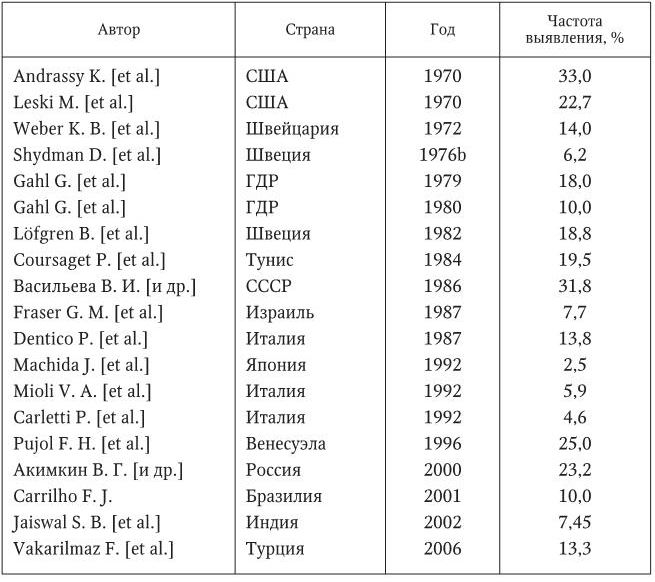
Частота выявления НВsАg у больных центров гемодиализа колеблется от 2,5 (Machida J. [et al.], 1992) до 33,0 % (Andrassy K. [еt al.], 1970) (табл. 1). Можно сделать вывод о различных уровнях инфицирования больных отделений и центров хронического диализа. Чаще всего такие случаи регистрировались в СССР, ГДР и Швеции. Распространенность инфекции определялась чувствительностью методов выявления, кратностью обследования пациентов и активностью действия факторов риска в пределах центра.
Таблица 1
Частота выявления НВsАg у пациентов центров гемодиализа по данным различных авторов
1.2. Клинические формы гепатита В у больных и персонала отделений гемодиализа
Клинические проявления ВГВ у пациентов, находящихся на гемодиализе, оказались весьма разнообразными. M. Leski [et al.] (1970) обследовали 67 человек, перенесших пересадку почек, 88 больных, получающих гемодиализ, и выявили 20,8 и 22,7 % носителей НВsAg. Клиническое течение варьировало: у носителей, переживших пересадку почек (71,4 %), инфекционный процесс протекал преимущественно без симптомов, у 55 % пациентов, получавших гемодиализ, наблюдались безжелтушные формы инфекции.
Так, при обследовании 65 больных с хронической почечной недостаточностью (ХПН) у 12 пациентов (18,4 %) обнаружены проявления гепатотропной инфекции, причем у половины из них отмечена желтушная форма, а у остальных – стертые и субклинические формы (Тареев Е. М. [и др.], 1972). Авторы считают, что стертые и субклинические формы связаны с низкой иммунологической реактивностью. Они склонны к затяжному, волнообразному течению вследствие иммунологических нарушений и персистирования вируса.
S. Polakoff [et al.] (1972), D. P. Sengar [et al.] (1975) показали, что лишь в 38,0 – 23,5 % случаев заболевания вирусным гепатитом у пациентов протекали в клинически выраженной форме, подтвердив данные M. Leski [et al.] (1970).
B. Löfgren [et al.] (1982) выявили 50 носителей HВsAg среди 196 больных отделения гемодиализа, в том числе 40 человек с хроническим и 10 – со здоровым носительством, причем у 77,5 % хронических и 21,3 % транзиторных носителей была повышена активность аланинаминотрансферазы (АлАТ).
M. Wiese [et al.] (1986) также подтвердили, что заболевания гепатитом В у пациентов, получающих гемодиализ, протекали преимущественно в безжелтушной форме и имели склонность к хронизации.
О. В. Соколова [и др.] (2001) провели углубленное исследование возникновения вирусных гепатитов у больных, подвергавшихся гемо- и перитонеальному диализу и установили, что соотношение острых и хронических форм гепатита В у больных отделения гемодиализа составляет1:4, причем хронический гепатит имел волнообразное течение, сопровождающееся периодическими подъемами АлАТ.
Пациенты с заболеванием почек в конечной стадии, подвергавшиеся диализу, имеют тяжелые повреждения печени и клеточного иммунитета, которые увеличивают риск развития хронической инфекции (Fabrizi F. [et al.], 2000). Примерно 20 % пациентов спонтанно избавляются от НВsAg, другие остаются хроническими носителями.
В настоящее время установлено восемь генотипов (А – Н) инфекции ВГВ. Распространение генотипов варьирует в зависимости от географической зоны. В США встречаются все известные генотипы, их частота оценивается следующим образом: А – 35 %,В – 22 %, С – 31 %, D – 10 %, Е – G – 2 %. В России преобладает генотип D. Последние исследования свидетельствуют о связи различных генотипов ВГВ с прогрессированием процесса и эффективностью терапии интерфероном. В то же время, несмотря на существенную необходимость, не представляется возможным широко внедрить генотипирование ВГВ в клиническую практику.
Взаимодействие вируса и иммунной системы позволило выделить четыре стадии течения хронической инфекции ВГВ: иммунная толерантность, иммунный клиренс, иммунный контроль и реактивация (Fattovich G. [et al.], 2007). Существует три основных клинико-серологических варианта заболевания: хронический НBеАg-позитивный гепатит, хронический НBeAg-негативный гепатит и неактивное носительство НВsАg. Следует отметить, что угнетение иммунной защиты у больных c ХПН накладывает свой отпечаток на клинические проявления ВГВ и способствует развитию хронического вирусного гепатита после острой фазы инфекции.
Клинические проявления инфекции ВГВ у больных с ХПН, получающих гемодиализ, имеют свои особенности. В диализных центрах около 50 % инфицированных больных становятся бессимптомными носителями вируса, у них не выявляются биохимические сдвиги, характерные для острого и хронического поражения печени. Мужчины более склонны к развитию носительства, это связано с их генетической предрасположенностью (гены, ответственные за образование антител, локализуются в Х-хромосоме, следовательно, у женщин имеется больше возможностей для образования антител). По мнению О. В. Соколовой [и др.] (2001), соотношение острых и хронических форм гепатита В у больных, получающих гемодиализ, составляет1:4.
Классическое течение острого ВГВ с желтухой, болями в конечностях, желудочно-кишечными расстройствами редко бывает у больных, находящихся на гемодиализе. Течение заболевания характеризуется малым числом желтушных форм и низкой активностью трансаминаз. Характерно преобладание легких безжелтушных форм. В классическом варианте заболевание постепенно начинается с преджелтушного (продромального) периода, его длительность – 2 – 4 нед. У рассматриваемой категории больных продромальный период прослеживается лишь в половине случаев и характеризуется усугублением слабости, усилением кожного зуда, снижением аппетита. Желтуха нарастает постепенно, однако тяжесть заболевания часто не соответствует ее выраженности. Длительность желтушного периода составляет от 2 – 4 нед. до 2 мес. Жалобы, свойственные этим пациентам в большей или меньшей степени, отсутствуют. Период разгара продолжается от 3 до 40 дней и сопровождается диспепсией, склонностью к кровоточивости, гипотонии. Печень увеличена у 50 % больных, активность аминотрансфераз не превышает 2 – 3 норм. Сравнительно нечасто желтушные варианты могут протекать тяжело, с развитием печеночной недостаточности и энцефалопатии. Из внепеченочных проявлений острого вирусного гепатита (ОВГ) чаще встречаются перикардит, миокардит, плеврит, асцит, полинейропатия и острый миелополирадикулоневрит (синдром Гийена – Барре). В период выздоровления желтуха постепенно регрессирует, размеры печени и селезенки нормализуются, кал и моча приобретают нормальную окраску (последнее соответствует состоянию кризиса болезни). Выздоровление может затянуться и иметь волнообразный характер.
По мнению Д. Е. Телегина [и др.] (2004), у больных, находящихся на гемодиализе, ОВГ имеет стертое, бессимптомное течение вследствие того, что инфекционный процесс развивается на фоне уже существующих субъективных и объективных проявлений ХПН. Доминирующим симптомом манифестных форм является холестатический синдром, который наблюдается у 71,4 % пациентов. Особенностью холестаза является проявление скорее субъективных признаков, чем степени нарушения пигментного обмена. Определяющим лабораторным тестом синдрома является увеличение активности гамма-глютамилтранспептидазы (ГГТП) и щелочной фосфатазы (ЩФ), наблюдается минимальная активность АлАТ. Белковосинтетическая функция печени, синтез факторов свертывания крови существенно нарушены. В целом, биохимическое исследование обнаруживает умеренное повышение аминотрансфераз и близкое к верхней границе нормы содержание билирубина. У больных, находящихся на гемодиализе, острый гепатит часто не распознается клинически. Нарушения иммунного статуса не позволяют элиминировать НВsАg и/или НBеАg из сыворотки многим пациентам отделений гемодиализа. Свойственные больным уремией нарушения иммунитета усугубляются на фоне инфекции ВГВ, приводят к отсроченной эволюции серологических маркеров. Так, временной интервал в 6 мес., которого обычно достаточно для констатации выздоровления или хронизации заболевания, увеличивается до 12 мес. и более у диализных больных. Лишь после истечения указанного срока можно говорить об исходе ОВГ.
Риск хронического носительства определяется у 1,5 – 2,0 % инфицированных, это объясняется влиянием уремических токсинов на общий метаболизм у больных с ХПН в терминальной стадии. Фактически 50,0 % инфицированных в диализных центрах становятся носителями НВеАg без проявления симптомов и биохимических сдвигов. У 10,0 – 15,0 % больных с персистирующей инфекцией ВГВ в общей популяции происходит спонтанная сероконверсия с первоначальным исчезновением из циркуляции дезоксирибонуклеиновой кислоты (ДНК) ВГВ, HBеAg и появлением антител к HBeAg (антител к HBe-антигену вируса гепатита В (анти-НВе)).
Приблизительно у 19,4 – 29,0 % пациентов, перенесших острый гепатит В (ОГВ), развивается хроническое течение заболевания. Хронический процесс имеет волнообразный характер, проявляющийся периодическим повышением активности АлАТ, отличается редкостью желтушных форм и низким уровнем трансаминаз. Е. М. Тареев [и др.] (1972) считают, что стертые и субклинические формы заболевания связаны с низкой иммунореактивностью. Это объясняется влиянием уремических токсинов на общий метаболизм у больных с ХПН в терминальной стадии. Изменения иммунного статуса у больных, находящихся на гемодиализе, являются фактором риска носительства хронического вирусного гепатита В (ХВГВ). По нашим данным, у этих больных наблюдаются более частые и тяжело протекающие инфекции, септические состояния. Манифестные формы ВГВ нередко характеризуются отсутствием продромального периода, выраженными проявлениями холестатического синдрома, диспепсическими проявлениями, гепатоспленомегалией.
Таким образом, особенностью клинического течения инфекционного процесса инфекции ВГВ у больных с ХПН – пациентов отделений диализа являются:
– легкое, безжелтушное или субклиническое течение у подавляющего числа больных, требующее активного выявления как специфическими, так и неспецифическими методами (маркеры вируса гепатита В, активность АлАТ);
– склонность к хроническому носительству, вернее к хроническому течению инфекции, у уремических больных. Частота хронического носительства в 5 – 8 раз выше, чем у неуремических больных. Примерно у 60 % диализных пациентов с инфекцией ВГВ развивается хронический гепатит с длительной персистенцией вируса и инфективностью. Эти два обстоятельства имеют важное эпидемиологическое значение, поскольку обеспечивают длительное нахождение вируса в отделении, поддерживая высокую напряженность эпидемической ситуации среди пациентов;
– отсутствие влияния носительства ВГВ на смертность от печеночной недостаточности и на отдаленную выживаемость.
Что касается клинического течения вирусного гепатита у персонала отделений диализа, то все исследователи отмечают, с одной стороны, невысокую частоту выявления носителей среди них, а с другой – более частое манифестирование инфекционного процесса и тяжелое клиническое течение заболеваний (Leski M. [et al.], 1970; Polakoff S. [et al.], 1972; Sengar D. P. [et al.], 1975). Например, D. P. Sengar [et al.] (1975) установили, что носительство НВsAg у персонала было кратковременным и не превышало 6 мес. Как правило, у медицинских работников заболевание ВГВ завершается полным выздоровлением.


