
Дэвид Бернс
Комплект книг «Терапия настроения»
Насколько хорошо проработаны эти теории, достаточно ли у них доказательств? Вовсе нет. Как я утверждал ранее, выдвинуть теорию очень просто, но доказать ее гораздо сложнее. На данный момент ни одну из этих теорий не удалось ни доказать, ни опровергнуть достаточно убедительно. К тому же не существует ни клинических, ни лабораторных испытаний, которые можно провести среди групп пациентов или отдельных пациентов, чтобы с достаточной точностью определить химический дисбаланс, вызывающий депрессию.
Основная ценность существующих теорий – в том, что они вдохновляют на дальнейшие исследования, уточняющие и углубляющие наши знания о работе мозга. Думаю, что со временем мы выдвинем более тщательно проработанные теории и создадим подходящие инструменты для их проверки.
Возможно, теперь вы думаете: «И это все? Ученые просто пытаются найти ответ на вопрос, возникает ли депрессия из-за избытка или недостатка того или иного трансмиттера или рецептора в мозге?» В каком-то смысле так и есть. Частично проблема состоит в том, что наши модели мозга все еще очень примитивны и, соответственно, наши теории о причинах депрессии также не очень точны.
Может оказаться, что возникновение депрессии не связано с проблемами в работе трансмиттеров или рецепторов. Однажды мы можем обнаружить, что депрессия – это проблема скорее «программного обеспечения», чем «железа». Иными словами, если у вас есть компьютер, то вы, вероятно, знаете, как часто они выходят из строя. Иногда это происходит из-за проблем с «железом», например ломается жесткий диск. Но гораздо чаще виной всему программное обеспечение: из-за какой-то ошибки программа дает сбой в определенных ситуациях. А что касается исследования мозга у пациентов с депрессией, возможно, мы ищем проблему в «железе» (например, врожденный химический дисбаланс), хотя в действительности она кроется в «программном обеспечении» (например, негативная модель мышления, связанная с обучением). Обе проблемы будут иметь органический характер, так как сопровождаются определенными процессами в головном мозге, но методы лечения будут радикально отличаться.
Другая важная проблема, с которой сталкиваются исследователи, – это дилемма «курица или яйцо». Изменения, которые мы регистрируем в мозге, – это причина или следствие депрессии? Чтобы проиллюстрировать эту проблему, давайте проведем мысленный эксперимент. Вообразите себе оленя в лесу. Он счастлив и доволен. Представьте, что у нас есть специальное устройство, которое позволяет нам наблюдать химическую электрическую активность в его мозге. Возможно, у нас есть футуристичное портативное устройство для улавливания активности мозга, способное работать на расстоянии, подобно лазерным радарам, которые полиция использует для регистрации скорости движения автомобилей. Однако олень не знает, что мы следим за активностью его мозга. Внезапно он замечает приближающуюся стаю голодных волков. Его охватывает паника. Наше устройство для отслеживания активности мозга улавливает мгновенные, но очень интенсивные изменения в электрической и химической активности мозга оленя. Являются ли эти химические и электрические измерения причиной или результатом его страха? Можно ли сказать, что олень напуган, потому что у него внезапно изменился химический баланс мозга?
Точно так же у пациентов в депрессии существуют разного рода электрические и химические изменения в мозге. Когда мы чувствуем счастье, злость или испуг, наш мозг переживает разительные изменения. Какие из них происходят из-за сильных эмоций, которые мы испытываем, а какие являются их причинами? Определить, где причина, а где следствие, – это одна из сложнейших задач, стоящих перед исследователями депрессивного расстройства. Эта проблема имеет решение, но она непроста, и сторонники уже имеющихся теорий о депрессии не всегда это признают.
Очевидно, исследования, которые необходимо провести для проверки любой из этих теорий, могут пугать. Одна из проблем связана с тем, что получить точную информацию о химических и электрических процессах внутри мозга очень сложно. Мы не можем просто вскрыть мозг пациента в депрессии и заглянуть внутрь! И даже если бы могли, то не знали бы, на что или как смотреть. Однако новые инструменты, такие как ПЭТ-сканирование (позитронная эмиссионная томография) и МРТ (магнитно-резонансная томография), делают такие исследования возможными. Ученые впервые смогут «увидеть» активность нейронов и химические процессы внутри человеческого мозга. Этот вид исследований все еще находится в зачаточном состоянии, но мы можем надеяться, что в следующем десятилетии нас ждет огромный прогресс в этом вопросе.
Как работают антидепрессанты?
Современная эра изучения химических процессов при депрессии начала стремительно набирать ход в начале 1950-х гг., когда исследователи провели испытания нового лекарства от туберкулеза под названием ипрониазид. Ипрониазид оказался неэффективен при лечении туберкулеза. Тем не менее исследователи заметили, что у пациентов, получавших лекарство, значительно повышалось настроение. Они выдвинули гипотезу, что ипрониазид может обладать свойствами антидепрессанта. Это привело к настоящему взрыву исследований, запущенных фармакологическими компаниями, которые хотели стать первыми в разработке и реализации лекарств, помогающих от депрессии.
Ученым было известно, что ипрониазид является ингибитором фермента МАО, который мы описывали ранее. Таким образом, это лекарство было отнесено к типу ингибиторов МАО, или коротко ИМАО. Было разработано несколько новых лекарств типа ИМАО, подобных ипрониазиду по химической структуре. Два из них, фенилзин («Нардил») и транилципромин («Парнат»), используются до сих пор. Третий антидепрессант ИМАО под названием селегилин (торговое название «Элдеприл») также был одобрен для лечения болезни Паркинсона. Он также иногда используется при лечении аффективных расстройств. Другие новые виды ИМАО, которые используются за границей, также могут продаваться в Соединенных Штатах.
Сейчас ИМАО прописывают не так часто, как ранее, потому что они могут вызывать опасные скачки артериального давления, если пациент сочетает их прием с определенными видами еды, например сыром. ИМАО также могут вызывать токсические реакции в сочетании с определенными лекарствами. Из-за этих угроз были разработаны более новые и безопасные виды антидепрессантов. Они работают совершенно иным образом, нежели ИМАО. Тем не менее ИМАО также могут оказаться крайне эффективны для некоторых пациентов в депрессии, если те не реагируют на другие лекарства. ИМАО могут быть абсолютно безопасны, если пациент и доктор четко следуют инструкциям.
Открытие ипрониазида помогло запустить новую эру биологических исследований депрессии. Ученым не терпелось выяснить, как действуют ИМАО. Им было известно, что ИМАО предотвращают распад серотонина, норэпинефрина и дофамина – трех химических передатчиков, которые сконцентрированы в лимбических зонах мозга. Ученые предположили, что недостаток одного или нескольких из этих веществ может вызвать депрессию и что антидепрессанты могут увеличивать уровень этих веществ. Так и возникли теории биогенных аминов.
Теперь давайте проверим, насколько хорошо вы разобрались в том, как работает мозг. Посмотрите еще раз на рисунки 17.1–17.3. Когда через пресинаптическое окончание проходит электрический импульс, серотонин выделяется в синаптическую щель. После того, как молекулы серотонина состыковались с рецепторами на постсинаптическом окончании, они возвращаются к пресинаптическому окончанию, где захватываются и уничтожаются ферментами МАО. Теперь спросите себя: что случится, если мы ограничим действие фермента МАО, то есть он перестанет уничтожать молекулы серотонина?
Как вы, возможно, догадались, серотонин продолжит накапливаться внутри пресинаптического окончания, потому что оно всегда производит молекулы серотонина. Если окончание не будет избавляться от избыточного серотонина, концентрация молекул внутри него может продолжать расти. Когда пресинаптическое окончание будет пропускать нервный импульс, он станет выбрасывать в заполненную жидкостью синаптическую область гораздо больше серотонина, чем обычно. Избыток серотонина в синапсе вызовет повышенную стимуляцию на постсинаптическом окончании. Это будет химическим эквивалентом повышения звука на радиоприемнике. Такой эффект антидепрессантов ИМАО изображен на рисунке 17.4.
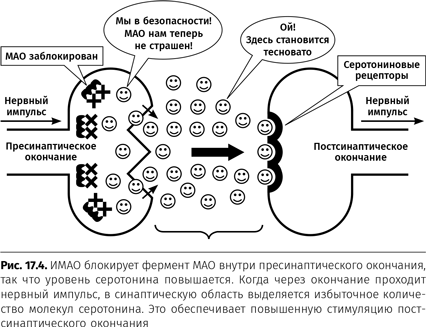
Может ли это быть причиной того, что препараты ИМАО вызывают повышение настроения? Возможно, так и есть, и ученые предполагают, что данный тип лекарств действует именно так. Исследования подтвердили, что, когда человек или животное употребляет ИМАО, уровень серотонина, норэпинефрина или дофамина в мозге повышается. Однако пока не установлено наверняка, является ли эффект этих антидепрессантов результатом повышения уровня одного из этих биогенных аминов или он вызван каким-либо иным воздействием данных лекарств на мозг.
Можете ли вы выдвинуть иную теорию о том, почему или как действуют ИМАО? Обязательно ли повышенное настроение является результатом более интенсивной стимуляции постсинаптического окончания или возможно другое объяснение? Прежде чем продолжить чтение, обдумайте то, что вы уже прочитали о даунрегуляции в предыдущем разделе, и попробуйте дать ответ.
Вероятно, вы помните, что воздействие на постсинаптические окончания через несколько недель может смениться противоположным эффектом. Через несколько недель избыток серотонина в синапсе может вызвать даунрегуляцию рецепторов постсинаптических серотониновых рецепторов, и именно даунрегуляция может объяснять действие антидепрессантов. (Помните: хотя одни ученые считают, будто депрессия является результатом дефицита серотонина, другие полагают, что она возникает вследствие избыточной серотониновой активности.) Если вы подумали именно об этом, это показывает, что вы действительно начали вникать в нейрохимию. За ответ на этот промежуточный контрольный вопрос вы получаете пятерку с плюсом!
Если вы предположили, что эффект антидепрессантов ИМАО может быть результатом действия какой-либо другой системы мозга, вы также получаете пятерку с плюсом. Теории о действии антидепрессантов не подтверждены фактами. Влияние препаратов ИМАО на мозг значительно сложнее простой модели, которая изображена на рисунке 17.4. Воздействие любого антидепрессанта, вероятно, не ограничено только одной конкретной областью или одним типом нейронов в мозге. Помните, что каждый нейрон соединяется со многими тысячами других нейронов, а все они, в свою очередь, соединяются с тысячами других. Когда вы принимаете антидепрессант, в вашем мозгу происходят масштабные изменения в многочисленных химических и электрических системах. Любое из них может улучшить ваше настроение. Попытка выяснить, как именно эти препараты работают, по-прежнему немного напоминает поиск иголки в стоге сена. Но на данный момент важно, что эти препараты действительно помогают некоторым пациентам в депрессии, и не имеет значения, как и почему они работают.
Как я упоминал ранее, с 1950-х гг. были разработаны и выведены на рынок несколько новых поколений антидепрессантов. В отличие от ИМАО, новые поколения антидепрессантов не вызывают нагромождения трансмиттеров, таких как серотонин, в пресинаптическом окончании, изображенном на рисунке 17.4. Вместо этого они имитируют эффект естественных трансмиттеров мозга, присоединяясь к рецепторам на поверхности пресинаптических или постсинаптических окончаний.
Чтобы понять, как новым поколениям антидепрессантов удается этого достичь, вспомните аналогию с замком и ключом. Молекула естественного трансмиттера подобна ключу, а рецептор на поверхности нерва – это замок. Ключ способен открыть замок только потому, что имеет определенную форму. Но будь вы волшебником, как знаменитый Гарри Гудини, вы могли бы легко подобрать отмычку и открыть замок без всякого ключа.
Антидепрессанты – это поддельный ключ, изготовленный фармацевтической компанией. Поскольку химикам известна трехмерная структура естественного трансмиттера, такого как серотонин, норэпинефрин или дофамин, они могут создавать новые лекарственные средства, имеющие очень похожую форму. Эти препараты будут состыковываться с рецепторами на поверхности окончаний и имитировать действие естественных передатчиков. Мозг не знает, что в замке находится антидепрессант, – мы его перехитрили, и теперь он полагает, что к рецептору на поверхности окончания прикрепился естественный трансмиттер.
В теории искусственный ключ – антидепрессант, прикрепляясь к рецептору, может играть одну из двух ролей. Он может либо открыть замок, либо занять скважину, не открывая его. Препараты, которые могут открыть замок, называются агонистами. Агонисты имитируют действие естественных трансмиттеров. Препараты, которые просто находятся в скважине, – это антагонисты. Антагонисты блокируют эффект естественных трансмиттеров и не позволяют им действовать.
Мы можем представить несколько способов, как антидепрессанты могут воздействовать на рецепторы на пресинаптическом и постсинаптическом окончании. Для целей нашего обсуждения представьте, что трансмиттер, используемый на пресинаптическом окончании, – это серотонин. (Однако те же рассуждения применимы к любому трансмиттеру.) Что случится, если заблокировать рецепторы на насосе обратного захвата? Пресинаптическое окончание больше не сможет всасывать серотонин из синапса обратно в нейрон. Каждый раз, когда через окончание проходит импульс, в синаптическую область будет выделяться все больше серотонина. В результате синапс будет переполнен серотонином.
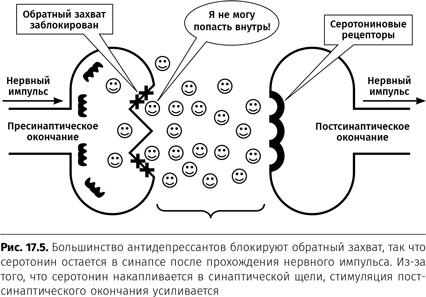
Именно так работают большинство антидепрессантов, прописываемых в настоящее время. Как вы видите на рисунке 17.5, они блокируют рецепторы обратного захвата на пресинаптическом окончании, так что трансмиттеры накапливаются в синаптической области. Конечный результат такого процесса подобен эффекту применения препаратов ИМАО, описанному выше. В обоих случаях уровень серотонина не повышается, так как молекулы накапливаются в синаптической области. Когда импульс проходит через пресинаптическое окончание, перемещаться к постсинаптическому окончанию и вызывать его стимуляцию будут больше молекул серотонина, чем обычно. Таким образом, мы снова «увеличиваем громкость» серотониновой системы.
Хорошо ли это? Поэтому ли препараты-антидепрессанты повышают наше настроение? Такова господствующая теория на данный момент, но на самом деле никто не знает точного ответа на этот вопрос.
Различные антидепрессанты блокируют различные аминные насосы, и одни из них имеют более специфичное действие, чем другие. Более старые «трициклические» антидепрессанты, такие как амитриптилин («Элавил»[25]) или имипрамин («Тофранил»[26]) и другие, блокируют обратный захват серотонина и норэпинефрина. («Трициклический» означает три колеса, как у трехколесного велосипеда, потому что химическая структура этих препаратов напоминает три соединенных кольца.) Таким образом, эти трансмиттеры накапливаются в мозге, когда вы принимаете один из этих препаратов. Одни трициклические антидепрессанты оказывают относительно более сильное воздействие на процесс обратного захвата серотонина, а другие – на обратный захват норэпинефрина. Препараты, сильнее влияющие на обратный захват серотонина насосами, называются серотонергическими, а препараты, относительно более сильно действующие на обратный захват норэпинефрина, – норадренергическими. Как вы думаете, как называется препарат, оказывающий более сильное воздействие на обратный захват дофамина? Если вы предположили, что «дофаминергический», то вы правы!
Некоторые антидепрессанты нового поколения, такие как флуоксетин («Прозак»[27]), отличаются от более старых поколений трициклических соединений тем, что оказывают более селективное и точное воздействие на обратный захват серотонина. Используя научные термины, можно сказать, что «Прозак» является высокосеротонергическим, потому что при его приеме молекулы серотонина будут накапливаться в большом количестве. Однако из-за того, что «Прозак» блокирует только обратный захват серотонина, уровень концентрации других трансмиттеров, таких как норэпинефрин и дофамин, не будет повышаться. Из-за своего селективного и направленного действия на механизм обратного захвата серотонина прозак относят к селективным ингибиторам обратного захвата серотонина (сокращенно СИОЗС). СИОЗС – еще одна пугающая аббревиатура с весьма простым значением. СИОЗС означает, что препарат блокирует только обратный захват серотонина, но не влияет на механизм обратного захвата других трансмиттеров.
Некоторые новые антидепрессанты не столь избирательны. Например, венлафаксин («Эффексор»[28]) блокирует обратный захват серотонина и норэпинефрина, так что его называют двойным ингибитором обратного захвата. Фармацевтическая компания, которая производит венлафаксин, развивает идею, что этот препарат может быть более эффективен, поскольку повышает уровень содержания сразу двух трансмиттеров: серотонина и норэпинефрина, а не одного. На самом деле это не такое уж и новшество. Как вы только что выяснили, большинство более старых и гораздо более дешевых антидепрессантов оказывают абсолютно такое же действие.
Кроме того, нет никаких доказательств, что венлафаксин работает лучше или быстрее, чем более старые препараты. Однако у него значительно меньше побочных эффектов, чем у некоторых более старых трициклических антидепрессантов. Это в некотором роде может оправдывать более высокую стоимость венлафаксина.
Итак, вы узнали о действии препаратов ИМАО и ингибиторов обратного захвата, таких как трициклические антидепрессанты и СИОЗС. Могут ли антидепрессанты оказывать еще какое-то воздействие? Если бы вы работали на фармацевтическую компанию и захотели создать абсолютно новый антидепрессант, какими бы свойствами он обладал? Один из вариантов – это создать препарат, который будет напрямую стимулировать серотониновые рецепторы на постсинаптическом окончании. Он станет имитировать эффект натурального серотонина, то есть будет, по сути, искусственным серотонином. Подобным образом действует буспирон («БусПар»[29]). Этот препарат напрямую стимулирует серотониновые рецепторы на постсинаптическом окончании. Буспирон был выведен на рынок несколько лет назад как первый препарат, который снижает тревожность и не вызывает привыкания, но также он действует как легкий антидепрессант. Однако его эффективность при лечении тревожных расстройств и депрессии не слишком высока. Из-за этого буспирон не пользуется большой популярностью.
Почему буспирон не оказался более эффективным при лечении депрессии? Ученые не знают ответа на этот вопрос. Однако помните, что в мозге существует по меньшей мере 15 видов серотониновых рецепторов. Все они выполняют различные функции, которые еще полностью не изучены. Возможно, препараты, которые стимулируют различные серотониновые рецепторы, могут оказывать более сильное действие при лечении депрессии. Вы, возможно, уже поняли: как только появляется новая информация о механизмах работы мозга, возникает еще большая путаница.
Если бы вы работали на фармацевтическую компанию, то могли бы также создать препарат, блокирующий серотониновый рецептор на постсинаптическом окончании, как показано на рисунке 17.6. Поскольку такие препараты будут блокировать действие натурального серотонина, они теоретически должны усиливать депрессию. В действительности препараты, которые блокируют серотониновые рецепторы, уже существуют. Два из них называются нефазодон («Созон») и тразодон («Дезирел»[30]). Хотя их относят к антагонистам серотонина, эти препараты также используются как антидепрессанты.
Определенные лекарства оказывают более комплексное воздействие на некоторые разновидности пре- и постсинаптических окончаний. Миртазапин («Ремерон»[31]) – это еще один антидепрессант нового поколения. Миртазапин блокирует серотониновые рецепторы на постсинаптическом окончании, а также стимулирует рецепторы норэпинефрина на пресинаптическом окончании. Это вызывает повышение выброса норэпинефрина на этих окончаниях. Так что, когда вы принимаете миртазапин, серотониновая система ослабляется, а норэпинефриновая усиливается.
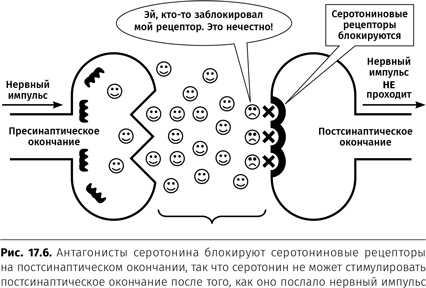
Воздействие таких антидепрессантов, как нефазадон, тразодон и миртазапин, прямо противоположно тому, которое можно предположить, исходя из серотониновой теории. Несмотря на то, что эти средства ослабляют серотониновую систему, они являются антидепрессантами. Как это возможно? Если вы чувствуете, что запутались, вы не одиноки. Вспомните, что в мозге существует несколько типов серотониновых рецепторов и все они обладают различными свойствами. Также вспомните о том, что между различными нейронными связями в мозге происходит множество быстрых и сложных реакций. Когда мы оказываем воздействие на одну нейронную систему в конкретной зоне мозга, то вызываем практически мгновенные изменения в тысячах или даже миллионах других нейронов в других зонах мозга. Согласно результатам последних исследований, даже сильнейшие специалисты из области нейронауки не имеют отчетливого понимания того, почему или как эти препараты приносят облегчение при депрессии.
Итак, подводя итоги, можно сказать, что большинство прописываемых сегодня антидепрессантов воздействуют на серотониновую, норэпинефриновую или дофаминовую системы. Некоторые из них высокоселективны и ориентированы на конкретную систему трансмиттеров, а другие оказывают влияние сразу на несколько систем. Однако воздействие антидепрессантов, прописываемых в настоящее время, на эти три системы не объясняет их благоприятный эффект достаточно последовательно или убедительно. Например, вы узнали, что одни антидепрессанты стимулируют повышение уровня серотонина, другие блокируют серотониновые рецепторы, а третьи, кажется, не оказывают на серотонин вообще никакого воздействия. И тем не менее все они обладают примерно одинаковой эффективностью. Очевидно, модели, которые я изобразил на рисунках 17.4–17.6, слишком упрощенные, а современные теории о том, как работают антидепрессанты, в лучшем случае неполны.
Я не хочу показаться пессимистом. Я вовсе не пытаюсь посеять сомнения в эффективности прописываемых антидепрессантов. Я просто хочу сказать, что теории о действии этих препаратов не принимают во внимание всех фактов.
К счастью, большинство исследователей в области нейронауки это признают, а фокус исследований значительно расширился. Вместо того, чтобы исследовать уровень того или иного биогенного амина, исследователи обращаются к более широкому набору стратегий, которые подразумевают изучение регуляционных механизмов всего мозга и разработку новых теории. Современные исследования изучают другие трансмиттеры мозга, свойства различных пре- и постсинаптических рецепторов, системы внутренней вторичной передачи, механизмы прохождения ионного тока через нервные мембраны, а также особенности нейроэндокринной и иммунной систем и нарушение биологических ритмов. Полагаю, что более всеобъемлющий подход, которого стараются придерживаться сегодня, со временем приведет к улучшению понимания регуляции настроения внутри мозга.
Развитие исследований мозга значительно ускорилось и в ближайшее десятилетие будет ускоряться еще больше. Следует надеяться, что новые исследования приведут к ряду улучшений, например:
• появлению клинических анализов для определения химического дисбаланса, который вызывает депрессию (если этот дисбаланс действительно присутствует);
• появлению анализов для определения генетических нарушений, которые повышают возникновения у некоторых людей депрессии, так же как для маниакально-депрессивного расстройства;
• разработке более безопасных препаратов с меньшим количеством побочных эффектов, хотя в данной области уже наблюдаются значительные улучшения;
• более эффективным и быстродействующим препаратам и способам психотерапевтического лечения;
• препаратам и способам психотерапевтического лечения, снижающим или полностью предотвращающим возвращение симптомов депрессии после выздоровления.
Хотя современный уровень понимания все еще весьма примитивен, в этом направлении предпринимаются серьезные шаги. Однажды они могут привести нас к обнаружению таинственной «черной желчи».







